Guía completa sobre qué es un puente de hidrógeno: Descubre cómo afecta a la vida y la química
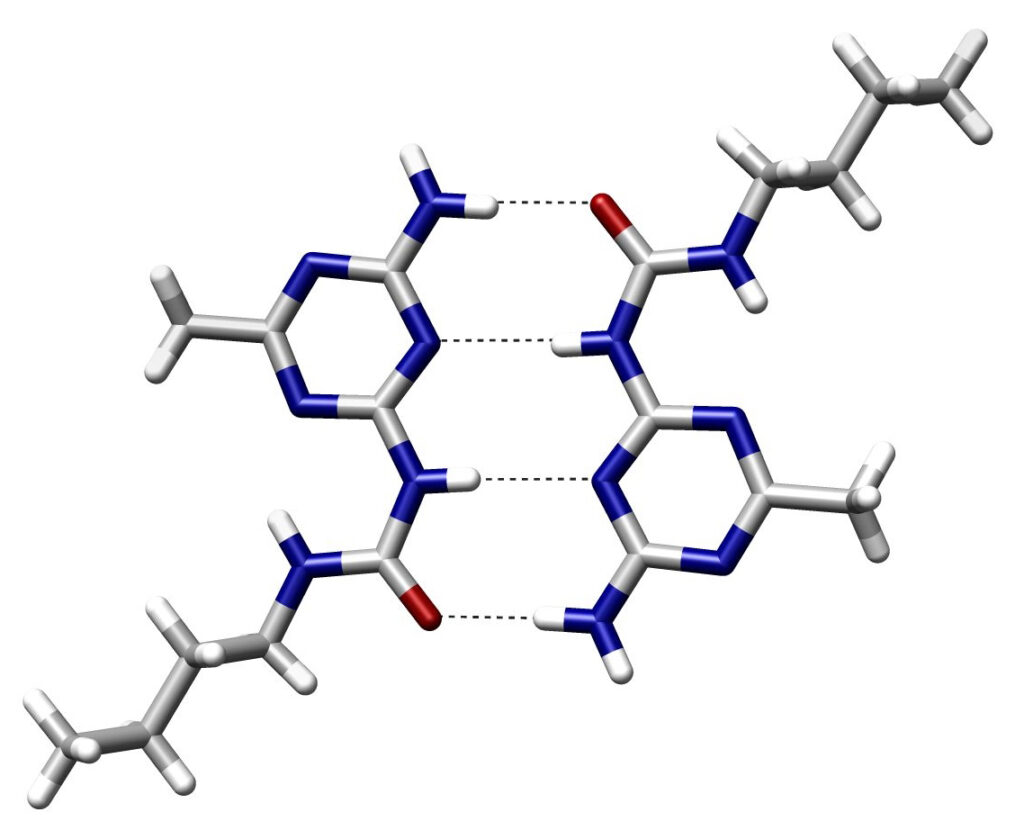
Los puentes de hidrógeno son fenómenos ampliamente estudiados en el campo de la química y la biología. Estas interacciones entre átomos de hidrógeno y otros átomos o moléculas son esenciales para entender muchos procesos químicos y biológicos, incluyendo las propiedades del agua, la estructura de las proteínas y el emparejamiento de bases en el ADN.
Exploraremos qué es un puente de hidrógeno, cómo se forma y cómo afecta a la vida y la química. Discutiremos su importancia en la estabilidad de las moléculas, su papel en la formación de estructuras biológicas y su influencia en las propiedades físicas y químicas del agua. También veremos algunos ejemplos específicos de puentes de hidrógeno en diferentes contextos químicos y biológicos. En definitiva, esta guía completa te proporcionará una visión sólida sobre uno de los conceptos fundamentales en la química y la biología.
- Qué es un puente de hidrógeno y por qué es importante en la vida y la química
- Cómo se forma un puente de hidrógeno y cuáles son sus características físicas y químicas
- Cuál es el papel del puente de hidrógeno en las moléculas de agua y cómo afecta a sus propiedades únicas
- De qué manera influye el puente de hidrógeno en la capacidad del agua para disolver diferentes sustancias y regular la temperatura de los organismos vivos
- Qué importancia tiene el puente de hidrógeno en la estructura y función del ADN y cómo esta interacción es crucial para la replicación y transcripción del material genético
- Cuáles son algunos ejemplos adicionales de cómo los puentes de hidrógeno desempeñan un papel vital en otras moléculas biológicas, como proteínas y carbohidratos
- De qué manera los investigadores están estudiando y aprovechando los puentes de hidrógeno en aplicaciones tecnológicas, como las celdas de combustible y los materiales superconductores
- Además de las celdas de combustible, otra área donde los puentes de hidrógeno están siendo ampliamente estudiados es en los materiales superconductores.
- Los puentes de hidrógeno no solo son fundamentales en la química y la biología, sino que también tienen una gran relevancia en diversas aplicaciones tecnológicas.
- Cuáles son las perspectivas futuras de investigación en torno a los puentes de hidrógeno y cómo podrían utilizarse en el desarrollo de nuevas terapias médicas o en la mejora de la eficiencia energética
- Cuáles son algunos consejos prácticos para comprender mejor los conceptos relacionados con los puentes de hidrógeno y su impacto en nuestras vidas diarias
- Dónde se puede encontrar más información sobre la temática de los puentes de hidrógeno y cómo se pueden aplicar en diferentes campos de estudio
- Preguntas frecuentes (FAQ)
- 1. ¿Qué es un puente de hidrógeno?
- 2. ¿Cuál es la importancia de los puentes de hidrógeno en la vida?
- 3. ¿Cómo afectan los puentes de hidrógeno a las propiedades del agua?
- 4. ¿Cómo influyen los puentes de hidrógeno en las interacciones entre moléculas?
- 5. ¿Se forman puentes de hidrógeno solo en compuestos orgánicos?
Qué es un puente de hidrógeno y por qué es importante en la vida y la química
Un puente de hidrógeno es una interacción química muy importante que se da entre un átomo electronegativo, como el oxígeno, nitrógeno o flúor, y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo. A pesar de ser una fuerza intermolecular débil en comparación con los enlaces covalentes o iónicos, los puentes de hidrógeno desempeñan un papel fundamental en la vida y la química.
En la biología, los puentes de hidrógeno son esenciales para muchas funciones importantes. Por ejemplo, contribuyen a la estructura secundaria del ADN y del ARN, ya que las bases nitrogenadas se unen mediante puentes de hidrógeno formando la famosa doble hélice del ADN. Sin estos puentes, nuestro material genético no podría replicarse de manera eficiente ni transmitir la información necesaria para la vida.
Además, los puentes de hidrógeno también son esenciales para la estructura de las proteínas. Las cadenas polipeptídicas se pliegan y adoptan su forma tridimensional gracias a la interacción entre los grupos amida, presentes en los aminoácidos, y los átomos de oxígeno e hidrógeno de otros residuos de aminoácidos cercanos. Este plegamiento determina la función de la proteína y su capacidad para interactuar con otras moléculas en el organismo.
En la química orgánica, los puentes de hidrógeno también tienen un impacto significativo. Por ejemplo, en la solubilidad de los compuestos orgánicos en agua. Muchos compuestos polares pueden formar puentes de hidrógeno con las moléculas de agua, lo que les permite disolverse y interactuar en soluciones acuosas. Además, estos puentes también influyen en las propiedades físicas y químicas de sustancias como los alcoholes, aldehídos y cetonas.
Es importante destacar que los puentes de hidrógeno no solo se limitan a la biología y a la química orgánica. También son relevantes en la química inorgánica y en otros campos científicos. En la química inorgánica, los puentes de hidrógeno pueden formarse entre moléculas polares o iónicas, lo que afecta las propiedades físicas y químicas de los compuestos. Además, en la física de materiales, los. puentes de hidrógeno juegan un papel importante en la estructura y propiedades de varios materiales, como los cristales y los materiales basados en hidruros metálicos.
Cómo se forma un puente de hidrógeno y cuáles son sus características físicas y químicas
Un puente de hidrógeno es una interacción intermolecular que se forma entre un átomo de hidrógeno enlazado covalentemente a un electronegativo, como el oxígeno, el nitrógeno o el flúor, y otro átomo electronegativo. Aunque esta interacción se llama "puente", cabe destacar que no hay enlace químico covalente entre los dos átomos involucrados en el puente de hidrógeno.
La formación de un puente de hidrógeno se debe a la polaridad de las moléculas y la interacción electrostática entre el átomo electronegativo y el átomo de hidrógeno parcialmente positivo. Este parcialidad positiva del hidrógeno resulta de la gran diferencia en electronegatividad entre el hidrógeno y el electronegativo al cual está enlazado. Cuando se establece un puente de hidrógeno, el átomo electronegativo donante de electrones (como el oxígeno en el agua) actúa como el receptor del puente, mientras que el hidrógeno se convierte en el donante. Esto genera una fuerte atracción entre los dos átomos, lo que da lugar a diversas propiedades físicas y químicas únicas.
Una de las características más importantes del puente de hidrógeno es su naturaleza direccional. La formación de un puente de hidrógeno requiere una alineación precisa entre el átomo electronegativo aceptor y el átomo de hidrógeno donante. Esto significa que el puente de hidrógeno no puede formarse en cualquier orientación, lo que limita las combinaciones posibles en un sistema dado.
Otra característica destacada del puente de hidrógeno es su fuerza intermolecular. Aunque es más débil que un enlace covalente, el puente de hidrógeno es considerablemente más fuerte que otras fuerzas intermoleculares, como las fuerzas dipolo-dipolo o las fuerzas de dispersión de London. Esta fuerza adicional se debe a la atracción electrostática entre los átomos parcialmente cargados de hidrógeno y electronegativo involucrados en la interacción.
Además de estas propiedades físicas, el puente de hidrógeno también juega un papel crucial en varias reacciones químicas y en la estabilidad de estructuras biológicas. En química, el puente de hidrógeno puede influir en la acidez y basicidad de compuestos orgánicos y ser utilizado para estabilizar intermediarios de reacción y transiciones. En biología, el puente de hidrógeno es fundamental para la estructura y función de moléculas biológicas importantes, como el ADN y las proteínas.
Un puente de hidrógeno es una interacción intermolecular que se forma entre un átomo electronegativo y un átomo de hidrógeno parcialmente positivo. Este tipo de enlace, aunque más débil que un enlace covalente, posee características físicas y químicas únicas, como su naturaleza direccional y su fuerza intermolecular superior. Además, el puente de hidrógeno desempeña un papel esencial en varias reacciones químicas y en la estabilidad de estructuras biológicas vitales.
Cuál es el papel del puente de hidrógeno en las moléculas de agua y cómo afecta a sus propiedades únicas
El puente de hidrógeno es un enlace intermolecular que se forma entre un átomo de hidrógeno con carga parcial positiva y un átomo electronegativo (como oxígeno, nitrógeno o flúor) con carga parcial negativa. Este tipo de enlace es responsable de las propiedades únicas del agua y su importancia en la vida y la química.
En una molécula de agua, cada uno de los dos átomos de hidrógeno forma un puente de hidrógeno con dos átomos de oxígeno distintos. Estos puentes de hidrógeno son responsables de mantener las moléculas de agua juntas en una estructura cristalina sólida a bajas temperaturas, formando el hielo. A medida que aumenta la temperatura, los puentes de hidrógeno se debilitan y las moléculas de agua pueden moverse más libremente, lo que resulta en la fase líquida del agua.
Además de sus propiedades de cohesión, los puentes de hidrógeno también juegan un papel crucial en las propiedades de solvatación del agua. Debido a la polaridad de los puentes de hidrógeno, las moléculas de agua pueden rodear y estabilizar iones y otros solutos polares. Esto les permite disolver muchas sustancias polares y desempeñar un papel vital en las reacciones químicas y biológicas en los organismos vivos.
Otra característica única del agua debido a los puentes de hidrógeno es su alta tensión superficial. Los puentes de hidrógeno permiten una atracción fuerte entre las moléculas de agua en la superficie, lo que crea una "piel" en la parte superior del líquido. Esta propiedad es especialmente importante en organismos acuáticos, como insectos que pueden caminar sobre el agua.
Los puentes de hidrógeno desempeñan un papel fundamental en las propiedades únicas del agua y su efecto en la vida y la química. Desde mantener las moléculas de agua juntas en estructuras sólidas hasta facilitar las reacciones y disoluciones, estos puentes son esenciales para nuestra comprensión de la química y el funcionamiento de los sistemas biológicos.
De qué manera influye el puente de hidrógeno en la capacidad del agua para disolver diferentes sustancias y regular la temperatura de los organismos vivos
El puente de hidrógeno es una interacción débil pero muy importante en el mundo de la química y la biología. Es un tipo de enlace que se forma entre un átomo de hidrógeno, que está unido covalentemente a otro átomo electronegativo (como oxígeno, nitrógeno o flúor), y un átomo cercano con una carga negativa o par de electrones no compartidos.
En el caso del agua (H2O), los puentes de hidrógeno son cruciales para sus propiedades únicas. El oxígeno tiene una alta electronegatividad, por lo que atrae más fuertemente los electrones compartidos en el enlace con el hidrógeno. Esto hace que el oxígeno tenga una ligera carga negativa parcial (δ-) y los hidrógenos una ligera carga positiva parcial (δ+).
Debido a estas cargas parciales, los átomos de oxígeno y de hidrógeno de diferentes moléculas de agua pueden atraerse entre sí mediante puentes de hidrógeno. Esto da lugar a la formación de una red tridimensional de puentes de hidrógeno en el agua líquida, lo cual es fundamental para muchas de sus propiedades.
Capacidad del agua para disolver diferentes sustancias
Uno de los efectos más importantes del puente de hidrógeno en el agua es su capacidad para disolver una amplia gama de sustancias polares y algunas no polares. El agua puede disolver fácilmente compuestos iónicos como la sal o el azúcar, así como moléculas polares como el etanol o el ácido acético.
Esto se debe a que las cargas parciales en los átomos de oxígeno e hidrógeno del agua interactúan con las cargas de otras sustancias, estableciendo puentes de hidrógeno entre ellas. Esta capacidad de formar puentes de hidrógeno permite que el agua "rompa" las fuerzas intermoleculares de otros compuestos y los rodee, disolviéndolos en una solución homogénea.
Además, el puente de hidrógeno también es responsable de la alta tensión superficial del agua, es decir, su resistencia a ser separada. Esto se debe a la fuerte red de puentes de hidrógeno presentes en la superficie del agua, que actúa como una "piel" que mantiene unida a la molécula de agua.
Regulación de la temperatura de los organismos vivos
Otra propiedad importante del agua relacionada con los puentes de hidrógeno es su capacidad para regular la temperatura de los organismos vivos. El agua tiene un calor específico alto, lo que significa que necesita absorber o liberar más energía para cambiar su temperatura en comparación con otras sustancias.
En este caso, los puentes de hidrógeno actúan como "amortiguadores" térmicos. Cuando la temperatura del ambiente aumenta, parte del calor se utiliza para romper los puentes de hidrógeno en el agua, lo que evita que la temperatura del organismo aumente rápidamente. Por el contrario, cuando la temperatura disminuye, se libera energía al formarse puentes de hidrógeno adicionales, lo que ayuda a mantener una temperatura relativamente estable.
Esta propiedad del agua es esencial para la vida, ya que permite a los organismos vivos mantener su homeostasis térmica, es decir, regular su temperatura interna en un rango adecuado para sus procesos biológicos.
Los puentes de hidrógeno son interacciones débiles pero fundamentales en el mundo de la química y la biología. En el caso del agua, estas interacciones son responsables de su capacidad para disolver diferentes sustancias y regular la temperatura de los organismos vivos. Comprender el papel de los puentes de hidrógeno nos ayuda a comprender mejor las propiedades y funciones de esta molécula vital.
Qué importancia tiene el puente de hidrógeno en la estructura y función del ADN y cómo esta interacción es crucial para la replicación y transcripción del material genético
El puente de hidrógeno es una interacción química sumamente importante en la estructura y función del ADN. Esta interacción juega un papel crucial en los procesos de replicación y transcripción del material genético, lo que a su vez tiene un impacto significativo en la vida y la química.
El ADN, o ácido desoxirribonucleico, es una molécula compuesta por dos cadenas complementarias enrolladas en una estructura de doble hélice. Cada cadena está formada por una serie de nucleótidos, que son unidades básicas compuestas por un azúcar (desoxirribosa), un grupo fosfato y una de las cuatro bases nitrogenadas: adenina (A), timina (T), citosina (C) y guanina (G).
La clave para entender la importancia del puente de hidrógeno en el ADN radica en la manera en que estas bases nitrogenadas se emparejan entre sí. La adenina siempre forma puentes de hidrógeno con la timina, mientras que la citosina se empareja con la guanina. Este emparejamiento específico es esencial para mantener la estructura de la doble hélice y garantizar la replicación y la transcripción precisas del ADN.
Cuando una célula necesita duplicar su ADN durante la replicación celular, las dos cadenas de la doble hélice se separan, y cada una sirve como molde para la formación de nuevas cadenas complementarias. A medida que cada nueva cadena se va ensamblando, las bases nitrogenadas se emparejan utilizando puentes de hidrógeno, asegurando que la secuencia original se conserve en las nuevas hebras de ADN.
Este proceso de reconocimiento y emparejamiento basado en puentes de hidrógeno es fundamental para mantener la integridad y la estabilidad del genoma. La precisión en la replicación y transcripción del ADN permite que cada célula hija reciba una copia exacta de la información genética, evitando errores que podrían tener consecuencias devastadoras, como mutaciones genéticas o enfermedades.
Además de su importancia en la replicación y transcripción de genes, el puente de hidrógeno también es crucial para otros procesos biológicos. Por ejemplo, en la síntesis de proteínas, el ADN proporciona el código genético necesario para la producción de proteínas a través del ARN mensajero (ARNm). Durante este proceso, el ARNm se une al ADN mediante puentes de hidrógeno en una reacción conocida como transcripción.
El puente de hidrógeno desempeña un papel fundamental en la estructura y función del ADN. Esta interacción química asegura la estabilidad, la precisión y la continuidad del material genético, permitiendo la replicación y transcripción precisa del ADN. Además, el puente de hidrógeno es esencial en otros procesos biológicos, lo que demuestra su importancia en la vida y la química.
Cuáles son algunos ejemplos adicionales de cómo los puentes de hidrógeno desempeñan un papel vital en otras moléculas biológicas, como proteínas y carbohidratos
Los puentes de hidrógeno no solo son fundamentales en la estructura del ADN y en la formación de la molécula de agua, sino que también desempeñan un papel crucial en otras biomoléculas como las proteínas y los carbohidratos.
En el caso de las proteínas, los puentes de hidrógeno están involucrados en su plegamiento tridimensional, lo que determina su estructura y función final. Estos puentes pueden formarse entre distintos aminoácidos presentes en la cadena polipeptídica. La interacción entre estos puentes de hidrógeno ayuda a estabilizar la estructura secundaria de la proteína, como las hélices alfa y las láminas beta.
Además, los puentes de hidrógeno también contribuyen a la interacción entre diferentes cadenas polipeptídicas, permitiendo la formación de estructuras más complejas como las proteínas globulares o los complejos proteicos.
En cuanto a los carbohidratos, los puentes de hidrógeno juegan un papel importante en la estabilidad y la función de estas moléculas. Por ejemplo, en la formación del glucógeno, una reserva energética en los animales, los puentes de hidrógeno se encuentran presentes enlazando las moléculas de glucosa, lo que le confiere su estructura ramificada y facilita su almacenamiento y posterior liberación de energía.
Otro ejemplo en el que los puentes de hidrógeno son fundamentales es en la formación de los disacáridos, como la sacarosa. La molécula de sacarosa está compuesta por una unión entre una molécula de glucosa y una de fructosa, y esta unión es posible gracias a los puentes de hidrógeno que se forman entre los grupos hidroxilo presentes en ambas moléculas.
Los puentes de hidrógeno son esenciales para la estructura y función de muchas moléculas biológicas, incluyendo proteínas y carbohidratos. Estos puentes permiten la formación de estructuras tridimensionales estables y contribuyen a la interacción entre diferentes componentes moleculares. Sin los puentes de hidrógeno, la vida tal como la conocemos no sería posible.
De qué manera los investigadores están estudiando y aprovechando los puentes de hidrógeno en aplicaciones tecnológicas, como las celdas de combustible y los materiales superconductores
Los puentes de hidrógeno son interacciones fundamentales en la química y la biología, pero también han demostrado ser esenciales en diversas aplicaciones tecnológicas. Desde el desarrollo de celdas de combustible hasta la búsqueda de materiales superconductores, los investigadores están explorando cómo aprovechar los puentes de hidrógeno para mejorar y revolucionar varios campos.
Una de las aplicaciones más prometedoras de los puentes de hidrógeno es en el ámbito de las celdas de combustible. Estas celdas funcionan convirtiendo la energía química contenida en compuestos como el hidrógeno y el oxígeno en energía eléctrica utilizable. Los puentes de hidrógeno desempeñan un papel crucial en este proceso, permitiendo la transferencia de iones de hidrógeno a través de membranas específicas. Gracias a esta transferencia controlada, las celdas de combustible pueden generar electricidad de manera más eficiente y sostenible.
Además de las celdas de combustible, otra área donde los puentes de hidrógeno están siendo ampliamente estudiados es en los materiales superconductores.
Los materiales superconductores son aquellos que, cuando se enfrían por debajo de una cierta temperatura crítica, adquieren propiedades eléctricas excepcionales, como la ausencia total de resistividad eléctrica. Estos materiales tienen aplicaciones potenciales en la transmisión de corriente eléctrica sin pérdidas y en la creación de dispositivos electromagnéticos más eficientes.
Los puentes de hidrógeno pueden desempeñar un papel determinante en el fenómeno de la superconductividad. En algunos materiales superconductores, los puentes de hidrógeno facilitan la formación de uniones débiles pero altamente cooperativas entre las moléculas o átomos del material, lo que permite la transferencia eficiente de electrones y la supresión de la resistividad eléctrica.
En la búsqueda de nuevos materiales superconductores, los investigadores están estudiando cómo modificar y controlar los puentes de hidrógeno para mejorar sus propiedades. Al comprender mejor los mecanismos que gobiernan la formación de estos puentes en diferentes compuestos, los científicos pueden diseñar materiales con características superconductoras más potentes y a temperaturas más altas.
Los puentes de hidrógeno no solo son fundamentales en la química y la biología, sino que también tienen una gran relevancia en diversas aplicaciones tecnológicas.
Desde el desarrollo de celdas de combustible más eficientes y sostenibles hasta la búsqueda de materiales superconductores capaces de revolucionar la transmisión de corriente eléctrica, los investigadores están aprovechando los puentes de hidrógeno para avanzar en ciencia y tecnología. A medida que se profundiza nuestra comprensión de estos puentes y de cómo manipularlos, es probable que veamos aún más avances en el futuro, llevando consigo importantes mejoras en diversos campos y proporcionando soluciones innovadoras a los desafíos actuales.
Cuáles son las perspectivas futuras de investigación en torno a los puentes de hidrógeno y cómo podrían utilizarse en el desarrollo de nuevas terapias médicas o en la mejora de la eficiencia energética
Los puentes de hidrógeno, una fuerza atractiva intermolecular, tienen múltiples aplicaciones en campos tan diversos como la biología, la química y la física. A medida que avanzamos en nuestro entendimiento sobre esta fascinante estructura, se nos presenta un panorama prometedor de avances futuros en investigación que pueden tener un impacto significativo en diversas áreas.
En el ámbito de la medicina, los puentes de hidrógeno están siendo objeto de estudio para comprender cómo afectan a las interacciones proteína-ligando y cómo estos conocimientos pueden ser utilizados en el desarrollo de nuevas terapias médicas. Se ha demostrado que los puentes de hidrógeno juegan un papel crucial en los procesos de reconocimiento molecular, proporcionando una base sólida para el diseño de fármacos más eficientes y específicos.
Otro campo en el que se están explorando las perspectivas futuras de investigación es la mejora de la eficiencia energética. Los investigadores están trabajando en el desarrollo de materiales que utilicen los puentes de hidrógeno para almacenar y liberar energía de una manera más eficiente. Estos materiales podrían tener aplicaciones en tecnologías emergentes, como las baterías de hidrógeno, lo que podría revolucionar la forma en que almacenamos y utilizamos la energía.
Investigación en sistemas biológicos
Uno de los campos más emocionantes de investigación en torno a los puentes de hidrógeno es su papel en la biología. Se ha descubierto que son fundamentales en la estructura del ADN y el ARN, lo que tiene implicaciones directas en la replicación y transcripción genética. Comprender cómo se forman y rompen los puentes de hidrógeno en el ADN y el ARN puede ayudarnos a desentrañar los mecanismos detrás de enfermedades genéticas y desarrollar nuevas formas de tratamiento.
Además, los puentes de hidrógeno también tienen un papel esencial en la estabilización de las estructuras proteicas. La forma en que las proteínas se pliegan y adoptan una conformación específica depende en gran medida de los puentes de hidrógeno. Investigar cómo interactúan estos puentes con las proteínas nos brinda información clave sobre su función y puede abrir nuevas vías para el diseño de fármacos dirigidos y terapias personalizadas.
Perspectivas futuras
A medida que continuamos investigando los puentes de hidrógeno, se abren cada vez más oportunidades emocionantes y prometedoras. En el ámbito biomédico, podríamos utilizar nuestros conocimientos sobre estos puentes para desarrollar terapias más eficaces y seguras, específicamente diseñadas para interactuar con dianas moleculares específicas. Además, la utilización de puentes de hidrógeno en tecnologías energéticas podría no solo permitirnos almacenar y liberar energía de manera más eficiente, sino también reducir nuestra dependencia de fuentes de energía no renovables.
Todavía hay mucho por descubrir y comprender sobre los puentes de hidrógeno y sus aplicaciones potenciales. La investigación futura en este campo sin duda nos llevará a nuevos avances y descubrimientos que impactarán positivamente en nuestras vidas. Es un emocionante momento para estar involucrado en esta área de estudio, ya que los puentes de hidrógeno continúan revelando sus secretos y posibilidades.
Cuáles son algunos consejos prácticos para comprender mejor los conceptos relacionados con los puentes de hidrógeno y su impacto en nuestras vidas diarias
Los puentes de hidrógeno son un concepto fundamental en química y biología, y entender su importancia es crucial para comprender cómo interactúan las distintas moléculas en nuestro entorno. En este artículo, te ofreceremos una guía completa sobre qué es un puente de hidrógeno, cómo afecta a la vida y la química, y algunos consejos prácticos para comprender mejor estos conceptos.
Qué es un puente de hidrógeno
Un puente de hidrógeno es una interacción débil entre un átomo de hidrógeno parcialmente positivo (H+) y un átomo electronegativo cercano, como oxígeno (O), nitrógeno (N) o flúor (F). Estos átomos electronegativos atraen los electrones compartidos del enlace covalente hacia ellos, generando una carga parcial negativa.
El átomo de hidrógeno, por otro lado, también tiene una carga parcial positiva debido a que el electrón compartido se desplaza ligeramente hacia el átomo electronegativo. Esta diferencia de cargas crea una atracción electrostática entre el átomo de hidrógeno y el electronegativo, lo que se conoce como puente de hidrógeno.
Importancia de los puentes de hidrógeno
Los puentes de hidrógeno son clave en muchas interacciones moleculares en la naturaleza. Por ejemplo, en el agua (H2O), cada molécula forma enlaces de puente de hidrógeno con otras cuatro moléculas de agua adyacentes. Estos puentes de hidrógeno son responsables de la estructura y las propiedades únicas del agua, como su alta capacidad calorífica y su elevado punto de ebullición.
Además del agua, los puentes de hidrógeno también juegan un papel crucial en la estabilidad de las estructuras secundarias de las proteínas, como las hélices alfa y las láminas beta. Estas estructuras se mantienen unidas gracias a los puentes de hidrógeno entre los grupos amida de los aminoácidos que conforman la proteína.
Impacto en la vida y la química
Los puentes de hidrógeno tienen un impacto significativo en la vida y la química en general. En la biología, son fundamentales para mantener la estructura tridimensional de moléculas como el ADN y el ARN, lo que permite la duplicación y transmisión de la información genética.
En términos más amplios, los puentes de hidrógeno influyen en muchas propiedades químicas y físicas de las moléculas. Por ejemplo, determinan la solubilidad de diferentes sustancias y pueden influir en las reacciones químicas. También son importantes en el estudio de la termodinámica de las interacciones moleculares y la cinética de la formación y rotura de enlaces químicos.
Consejos prácticos para comprender los puentes de hidrógeno
Si estás interesado en profundizar en el tema de los puentes de hidrógeno, aquí te ofrecemos algunos consejos prácticos para comprender mejor estos conceptos:
- Lee libros de química y biología: Existen numerosos textos especializados que explican en detalle la importancia de los puentes de hidrógeno. Estos libros pueden brindarte una visión más completa y detallada sobre este tema.
- Realiza experimentos caseros: Puedes realizar experimentos sencillos en casa que ilustren la relevancia de los puentes de hidrógeno. Por ejemplo, puedes observar cómo se forman gotas en el borde de un vaso con agua o crear modelos moleculares para entender mejor las interacciones a nivel atómico.
- Busca recursos en línea: La web ofrece una amplia gama de recursos educativos, como videos, tutoriales y presentaciones interactivas, que pueden ayudarte a visualizar y comprender mejor los puentes de hidrógeno. Explora diferentes fuentes confiables y asegúrate de obtener información precisa y actualizada.
- Participa en actividades prácticas: Inscríbete en talleres, cursos o conferencias donde puedas realizar actividades prácticas relacionadas con los puentes de hidrógeno. La participación activa te permitirá experimentar de primera mano estos conceptos y facilitará una comprensión más profunda.
Los puentes de hidrógeno son interacciones débiles pero cruciales en diversas áreas científicas, desde la biología hasta la química. Comprender mejor estos conceptos puede abrir las puertas a un mundo fascinante de descubrimientos y aplicaciones en diferentes campos. Esperamos que esta guía completa te haya ayudado a desentrañar los misterios de los puentes de hidrógeno y a apreciar su importancia en nuestras vidas diarias.
Dónde se puede encontrar más información sobre la temática de los puentes de hidrógeno y cómo se pueden aplicar en diferentes campos de estudio
Para ampliar tus conocimientos sobre el fascinante mundo de los puentes de hidrógeno y su aplicación en diversos campos de estudio, existen diversas fuentes donde puedes encontrar información detallada y especializada. A continuación se mencionan algunas de estas fuentes:
Libros y manuales académicos
Una forma tradicional pero efectiva de obtener información más completa sobre los puentes de hidrógeno es buscar libros y manuales académicos escritos por expertos en química, biología y otras disciplinas relacionadas. Estos recursos suelen ofrecer una visión profunda y exhaustiva sobre la estructura, formación y aplicación de los puentes de hidrógeno en diferentes contextos.
Revistas científicas especializadas
Las revistas científicas especializadas son otra fuente valiosa para encontrar información actualizada sobre el tema. En estas publicaciones, investigadores y científicos comparten los resultados de sus estudios e investigaciones relacionadas con los puentes de hidrógeno. Algunas de las revistas más reconocidas en este campo incluyen "Journal of the American Chemical Society", "Nature Chemistry" y "The Journal of Physical Chemistry".
Bases de datos científicas
Además de las revistas científicas, también es posible acceder a bases de datos en línea que recopilan artículos científicos y publicaciones relacionadas con los puentes de hidrógeno. Estas bases de datos permiten realizar búsquedas específicas y filtrar la información según criterios como fecha, autor o área temática. Algunas de las bases de datos más populares en este campo son "PubMed", "SciFinder" y "Google Scholar".
Conferencias y congresos científicos
Asistir a conferencias y congresos científicos es una excelente manera de mantenerse actualizado sobre los avances más recientes en el estudio de los puentes de hidrógeno. Estos eventos reúnen a expertos de todo el mundo que comparten sus investigaciones y descubrimientos durante ponencias y presentaciones. Además, brindan la oportunidad de establecer contactos con profesionales del campo y participar en discusiones académicas de alto nivel.
Recursos educativos en línea
En la era digital, existen numerosos recursos educativos en línea que puedes consultar para aprender más sobre los puentes de hidrógeno. Plataformas de aprendizaje como Coursera, Khan Academy y edX ofrecen cursos gratuitos o de pago sobre química, bioquímica y otras disciplinas relacionadas, donde podrás encontrar módulos específicos dedicados al estudio de los puentes de hidrógeno. Además, muchas universidades e instituciones académicas también tienen disponibles recursos educativos en línea, como videos, tutoriales y presentaciones en diapositivas.
Si deseas profundizar en el conocimiento sobre qué es un puente de hidrógeno y cómo afecta a la vida y la química, tienes a tu disposición una amplia gama de fuentes de información. Ya sea a través de libros, revistas científicas, bases de datos, conferencias o recursos en línea, podrás sumergirte en el fascinante mundo de los puentes de hidrógeno y descubrir su importancia en el funcionamiento de los sistemas biológicos, la formación de compuestos químicos y mucho más.
Preguntas frecuentes (FAQ)
1. ¿Qué es un puente de hidrógeno?
Es una interacción química débil que se forma entre un átomo de hidrógeno y un átomo electronegativo (como el oxígeno, el nitrógeno o el flúor) de una molécula diferente.
2. ¿Cuál es la importancia de los puentes de hidrógeno en la vida?
Los puentes de hidrógeno son fundamentales para muchas biomoléculas y procesos biológicos, como la estructura del ADN, la formación de proteínas y la actividad de las enzimas.
3. ¿Cómo afectan los puentes de hidrógeno a las propiedades del agua?
Los puentes de hidrógeno en el agua le dan sus propiedades únicas, como su alta tensión superficial, su capacidad para disolver muchas sustancias y su capacidad para regular la temperatura.
4. ¿Cómo influyen los puentes de hidrógeno en las interacciones entre moléculas?
Los puentes de hidrógeno pueden influir en la formación de redes tridimensionales de moléculas, como en los cristales, y también pueden afectar las interacciones entre moléculas en reacciones químicas.
5. ¿Se forman puentes de hidrógeno solo en compuestos orgánicos?
No, los puentes de hidrógeno se pueden formar tanto en compuestos orgánicos como en compuestos inorgánicos, siempre que haya átomos electronegativos y átomos de hidrógeno disponibles para interactuar.

Entradas relacionadas